1.-Definición:
-La química orgánica es la química del carbono y de sus compuestos.
-La Química orgánica ó Química del carbono es la rama de la química que estudia una clase numerosa de moléculas que contienen carbono formando enlaces covalentes carbono-carbono o carbono-hidrógeno, también conocidos como compuestos orgánicos.
-La Química orgánica es la rama de la química que estudia una clase numerosa de moléculas que contienen carbono formando enlaces covalentes
Por tanto el carbono es un elemento esencial en todos los seres vivientes.
http://es.wikipedia.org/wiki/QuÃmica_orgánica
http://www.quimicaorganica.net/
1.1.- Importancia de la química orgánica.
-Los seres vivos estamos conformados por varios tipos de compuestos orgánicos, en todos ellos la base principal es el carbono, los compuestos organicos esta ligado con lo que nos rodea como la ropa, el jabon, el champú…
http://www.quimicaorganica.net/
2.-Estudios del átomo de Carbono y de sus componentes
2.1Propiedades físicas.
En su forma elemental, el carbono se encuentra en las formas carbón, grafito, diamante, fullereno y nanotubos. Éstos son materiales con propiedades muy diferentes, pero a nivel microscópico solo difieren por las disposiciones geométricas de los átomos de carbono.
Punto de fusión.- La fusión se produce cuando se alcanza una temperatura a la cual la energía térmica de las partículas es suficientemente grande como para vencer las fuerzas intracristalinas que las mantienen en posición.
Fuerzas intermoleculares.- estas fuerzas parecen ser de naturaleza electrostática, en las que cargas positivas atraen cargas negativas. Hay dos clases de fuerzas intermoleculares: interaccione dipolo-dipolo y fuerzas de Van der Waals
Punto de ebullición.- La ebullición implica la separación de moléculas individuales, o pares de iones con carga opuesta, del seno del líquido. Esto sucede cuando se alcanza una temperatura suficiente para que la energía térmica delas partículas supere las fuerzas de cohesión que las mantienen en el líquido.
http://132.248.103.112/qo1/MO-CAP1.htm
2.2 propiedades químicas.(explicación y gráficos de cada una)
LA COVALENCIA: Esta propiedad consiste en que los 4 orbitales híbridos son de Igual intensidad de energía y por lo tanto sus 4 enlaces del carbono son iguales. Y de igual clase. Esto significa que el carbono ejerce la misma fuerza de unión por sus 4 enlaces, un buen ejemplo seria el del metano. En el metano los 4 hidrógenos son atraídos por el carbono con la misma fuerza ya que sus 4 enlaces son de la misma clase.


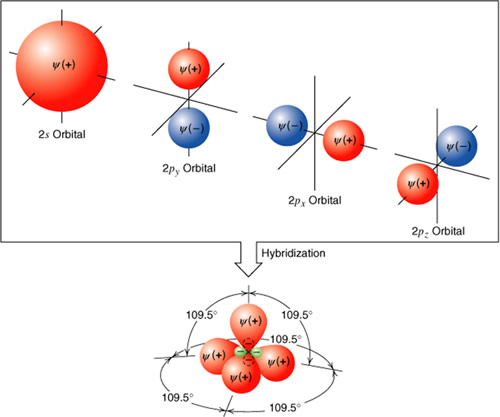
LA HIBRIDACION: Consiste en un reacomodo de electrones del mismo nivel de energía (orbital s) al orbital p del mismo nivel de energía. Esto es con el fin de que el orbital p tenga 1 electrón en "x", uno en "y" y uno en "z" para formar la tetravalencia del carbono. Se debe tomar en cuenta que los únicos orbitales con los cuales trabaja el Carbono son los orbitales "s" y "p".
LA AUTOSATURACION: Es la capacidad del átomo de carbono para compartir sus electrones de valencia consigo mismo formando cadenas carbonadas, esta propiedad es fundamental en el carbono y lo diferencia de los demás elementos químicos. Al compartir sus electrones con otros átomos de carbono puede originar enlaces simples, dobles, o triples de tal manera que cada enlace representa un par covalente y comparten dos y tres pares de electrones.

El carbono y sus compuestos se encuentran distribuidos ampliamente en la naturaleza. Se estima que el carbono constituye 0.032% de la corteza terrestre. El carbono libre se encuentra en grandes depósitos como hulla, forma amorfa del elemento con otros compuestos complejos de carbono-hidrógeno-nitrógeno. El carbono cristalino puro se halla como grafito y diamante.
3.- Funciones químicas
3.1.-Definición.-
Es un conjunto de compuestos que tienen propiedades muy parecidas en virtud a que sus moléculas contienen uno o más átomos iguales. Representación convencional de los elementos que forman un compuesto o molécula. En la fórmula química se indican los elementos presentes en cada molécula y como subíndice junto a cada uno el número de átomos de ese elemento presentes.
Peso atómico es el número de electrones que tiene un determinado elemento químico.
C6 = 1s2 ,2s2, 2pX1, 2pY1
H= 1s1
La ley del octeto nos dice que al unirse dos átomos ambos deben quedar con 8 electrones.
Enlaces entre átomos
Los enlaces covalentes entre átomos de carbono se diferencia en su fortaleza, longitud y su geometría. La fortaleza de un enlace se mide por la cantidad de energía que es necesario aplicar parar romperlo.
La longitud de un enlace es la distancia que separa los centros de los dos átomos que están unidos.
La geometría es la orientación de las moléculas en el espacio.
Cadenas carbonadas


Formulas:
Desarrollada o estructural: muestra la ubicación de los átomos de carbono que forman la molécula

CARBONOS PRIMARIOS: poseen 3 hidrógenos porque se unen a otros átomos de carbono mediante enlaces simples.
CARBONOS SECUNDARIOS: poseen 2 hidrógenos porque se unen a otros átomos de carbono mediante 1 enlace simple se une a otros dos carbonos mediante enlaces dobles.
CARBONOS TERCIARIOS: poseen 1 hidrógeno porque se une a un átomo de carbono mediante un enlace simple y a otro mediante un enlace doble; o se une a un átomo de carbono mediante un enlace triple.
CARBONOS CUATERNARIOS: no poseen hidrógenos, porque se unen con 2 átomos de carbono mediante enlaces dobles, o mediante un enlace triple y un simple, o mediante un enlace cuádruple.
Funciones química
Son un conjunto de compuestos que tienen una propiedad en común, debido a que poseen elementos similares.
Hidrocarburos: compuestos binarios, formados por carbono e hidrógeno.
Oxigenadas: alcohol, eters, aldehidos, acidos orgánicos, esteres, sales orgánicas, acetonas.
Nitrogenadas: aminas, iminas, amidas, cianuro, aminoácidos, nitrilos.
Hidrocarburos:
H3C – CH3 ----> C2H6
H2C = CH2 ----> C2H4
HC == CH ----> C2H2
C – C – C – C – CH3 H3 H2 H2 H2 | C – C = C – C – CH3 H3 H H H2 | H3 C – C – C ≡ C – C H3 H2 |
C5H12 | C5H10 | C5H8 |
Clasificación:
Alcanos (enlaces simples) CnH2n+2
Ejemplo
C10H22 ; C13H23
Alquenos (enlaces dobles) CnH2n
Ejemplo
C10H20 ; C13H22 con 3 enlaces dobles
Alquinos (enlaces triples) CnH2n-2
Ejemplo
C10H18 ; C13H12 con 4 enlaces triples
* Cada enlace doble disminuye 2 hidrógenos y cada enlace cuádruple disminuye 4 hidrógenos.
Ejemplos
C5H12 si todos los enlaces son simples
C5H4 con 4 enlaces dobles
C5H4 con 2 enlaces triples
C7H16 si todos los enlaces son simples
C7H10 con 3 enlaces dobles
C7H4 con 3 enlaces triples
Nomenclatura
# Carbonos | Prefijo | Sufijo |
1 | MET | ANO ENO INO |
2 | ET | |
3 | PROP | |
4 | BUT | |
5 | PENT | |
6 | EX | |
7 | HEPT | |
8 | OCT | |
9 | NON | |
10 | DEC | |
11 | UNDEC | |
20 | EICOS |
Regla para enumerar: se nuera de arriba hacia abajo, o de izquierda a derecha, si se da el nombre.



RADICALES ALQUILOS
En cadenas abiertas lineales o acíclicas
CnH2n+1

CnH2n-1

CnH2n-3

PENTADECILO
C15H32.. ILO=-1 > C15H31
TETRADECADIINILO
C14H30…DIIN = -4, ILO=-1…C14H21
PENTADECENEILO
C15H32…ENE=-2 ILO=-1…C15H29
TRIDECATRIENDIINILO
C13H28… TRIEN=-6 DIIN=-8,ILO=-1…C13H13
En cadenas cerradas o cíclicas
En las cadenas cíclicas no funcionan las reglas, el número de hidrógenos siempre será el doble del número de carbonos (en el caso de ser alcanos)
Ciclopropano C3H6

Ciclopropilo C3H5’

CICLOPENTENILO C5H7’

Para enumerar se comienza desde el extremo superior en sentido horario, en el caso de una cadena en forma de cuadrado se comienza desde la esquina superior derecha.
Si todos los enlaces son simples la cadena principal es la que posee mayor número de átomos de carbono.
Se enumera desde la parte más cercana a la cadena lateral.
Las cadenas laterales son radicales.




Aldehídos
VII A


*Hidrocarburos alógenos; es un hidrocarburo en el cual se remplaza un hidrogeno por un alógeno.
Di cloro Propeno
C3H4Cl2

Tri bromo butano (en formula global)
C4H5Br3
Tri bromo ciclobuteno
C4H3Br3








Formula funcional: se destacan los grupos funcionales (carbonilos en el siguiente caso)
C6H4O2 = C4H2 (CHO)2
En los hidrocarburos no se puede usar la formula funcional, porque al contrario de los aldehídos no hay presencia de grupos funcionales.
Representar el tridecatrienoinodial en formula funcional
C11H12 (CHO)2
*Un carbonilo reduce 3 hidrógenos porque el átomo de oxigeno remplaza 2 hidrógenos.
Eicosapentenodiinodial en formula funcional
C18H18(CHO)2
Butial 3 – exenil5 – octadienilal 8, tetradecadieno 7-9-ino11 AL1 (formula semidesarrollada y funcional)

Octadienilal en formula funcional
-C7H10CHO2
Los hidrocarburos de enlaces dobles o triples son hidrocarburos no saturados
Un oxigeno remplaza dos hidrógenos de un hidrocarburo primario, y remplaza dos hidrocarburos en un hidrocarburo secundario (CH2)
Acetonas
Propanona C2H6CO

Grupo cetónico o cetonilo, característica de la función oxigenada cetonas.
El número de acetonas depende del número de carbonos.

El sufijo –ona disminuye dos átomos de hidrógeno
Pentenona
C4H8CO
Pentenilona en formula semidesarrollada
-C4H7CO

CICLOBUTENONA
C3H4CO
CICLOBUTENILONA
-C3H3CO
HEPTENINODIONAL
(*
C4H3(CO)2 CHO
HEPTENINILDIONAAL
C4H2(CO)2 CHO
Función Alcohol


En una cadena carbonada hay oxidrilos como haya hidrógenos.

Fenol

Anillo bencénico

Cuando el oxígeno remplaza al hidrogeno en el benceno se forma fenol.




Función éteres
Para formar un éter se necesitan dos alcoholes monoles (1oxidrilo = alcohol monol, 2 o más oxidrilos= alcohol poliol)

Ejemplos



Ácidos orgánicos
(1oxidrilo = monoicos, 2 oxidrilos= dioicos)
Se da solo si hay presencia de carbonos primarios.

El sufijo –oico disminuye 3 Hidrógenos

Monoicos importantes
Acido etanoico o acético
Acido propanoico o propionico
Acido butenoico o butírico
Acido pentanoico o Vaerico
Dioicos importantes
Acido etanoico u oxalico


Función esteres
El sufij –oico cambia por el sufijio –oato

Un ester se forma por la unión de un ácido orgánico y un alcohol.
Cuando el ácido orgánico pierde un hidrógeno del grupo carboxilo y el alcohol pierde el oxidrilo, se forma la molécula de agua; quedando dos electrones libres que se compartirán.

Nombres comerciales de los principales ácidos orgánicos
Ácidos inferiores
Acido Metanoico o fórmico
Acido etanoico o acético
Acido propanoico o propiónico
Acido butenoico o butírico
Acido pentanoico o valérico
Acido exanoico o caproico
Acido heptanoico o enántico
Acido octanoico o caprílico
Ácidos grasos o superiores
Acido dodecanoico o laurico
Acido tetradecanoico o mirístico
Acido exadecanoico o palmitico
Acido heptadecanoico o margarico
Acido octadecanoico o estearico
Acido etano dioico o oxádico
Acido propano dioico o masónico
Acido butano dioico o succírico

Estearato de exenil
C17H35COOH + C6H11OH
C17H35COO.C6H11 + H2O
Caprilato de nonadieninil
C7H15COOH + C9H11OH
C7H15COO.C9H11 + H2O

Acido palmítico (exadecanoico) + glicerina

Función Sales Orgánicas (ácido orgánico + hidroxilo /bases/alcalis)


EJEMPLO
Valerato de potasio
C4H9COOH + KOH
C4H9COOK + H2O

Funciones Nitrogenadas
